
Увеличение средней продолжительности жизни (в развитых странах до 75–80 лет) является, без сомнения, выдающимся достижением современной цивилизации. Однако «нагрузкой» к желанному долголетию стало неуклонное старение населения, породившее целый ряд серьезных социальных, экономических и медицинских проблем. Эксперты отмечают увеличение числа пожилых людей с хроническими нейродегенеративными заболеваниями, для большинства из которых отсутствуют радикальные методы лечения, позволяющие обратить вспять или хотя бы остановить патологический процесс. Одно из них, наиболее распространенное, в 1817 году описал английский врач Джеймс Паркинсон
Что такое болезнь Паркинсона
Болезнь Паркинсона — хроническое прогрессирующее дегенеративное заболевание центральной нервной системы, клинически проявляющееся нарушением произвольных движений. В настоящее время распространенность болезни Паркинсона в целом составляет 1–2 на 1000 человек населения. В возрастной категории старше 70 лет недуг поражает одного из 100, старше 80 лет — одного из 50 человек. Заболеваемость паркинсонизмом не зависит от половой и расовой принадлежности, социального положения и места проживания. Средний возраст начала болезни — 55 лет, в то же время у 10% больных заболевание дебютирует в возрасте до 40 лет.
Дрожание рук и ног (тремор), скованные, замедленные движения, ослабление тонуса мышц, нарушение равновесия при сохранении чувствительности и интеллекта — так в своем «Эссе о дрожательном параличе» доктор Джеймс Паркинсон (1755–1824) описал основные симптомы заболевания, позже названного его именем. Интересно, что шестеро больных, чьи истории болезни легли в основу «Эссе», не были пациентами Паркинсона. Врач фиксировал развитие внешних проявлений заболевания, на протяжении нескольких лет наблюдая за ними во время ежедневных прогулок. Он также обратил внимание на некоторые специфические для «дрожательного паралича» симптомы: непроизвольные движения пальцев, напоминающие «счет монет», и характерную позу просителя.
Термин «дрожательный паралич» был придуман не самим Паркинсоном, а писателем Джоном Обри (1626–1697). В своем биографическом труде «Жизнь мистера Томаса Гоббса из Малмсбери» он назвал дрожательным параличом тяжелый прогрессирующий недуг, в почтенном возрасте поразивший известного английского философа.
В 1861 году французский невропатолог Жан-Мартен Шарко (1825–1893) и физиолог Альфред Вульпиан (1826–1887) — опубликовали совместный труд, в котором дополнили описание болезни, данное Паркинсоном, собственными наблюдениями и, отдавая должное работам английского коллеги, впервые использовали термин «болезнь Паркинсона».
Заслуга Паркинсона в создании первого точного и яркого «портрета» заболевания, хотя упоминания о схожих недугах встречаются в древних и средневековых медицинских трактатах, летописях и мемуарах, в текстах Ветхого и Нового Заветов. В античных источниках приведены и схемы лечения, включающие самые разнообразные мероприятия — от игры в мяч и прогулок на свежем воздухе до применения лекарств на основе семенников бобра. Первое эффективное средство, смягчающее симптомы и замедляющее развитие болезни Паркинсона, предложено в индийских священных писаниях, называемых Ведами. Это и другие нервные заболевания древние индусы советовали лечить бобами растения Mucuna pruriens, называемого также бархатной фасолью. Уже в ХХ веке выяснилось, что указанные бобы содержат терапевтическую дозу леводопы — ныне широко применяемого в синтетическом виде противопаркинсонического лекарственного средства.
Причины болезни Паркинсона
Нейронные тайны
Несмотря на пристальное внимание специалистов к проблеме нейродегенеративных заболеваний, причины болезни Паркинсона до конца не выяснены. Не вызывает сомнения, что паркинсонические нарушения полиэтиологичны. Поскольку некоторые признаки заболевания наблюдаются и при нормальном старении, это позволяет сделать вывод, что одним из причинных факторов паркинсонизма может быть возрастное снижение количества мозговых нейронов. В то же время компенсаторные возможности мозга настолько велики, что клинические симптомы развиваются лишь после гибели 80% всех нейронов головного мозга.
Болезнь Паркинсона носит преимущественно спорадический характер, однако при наличии этого заболевания у ближайших родственников риск развития данной патологии возрастает в два раза. В связи с этим многие ученые настаивают на решающей роли наследственных факторов в возникновении болезни.
Болезнь Паркинсона прогрессирует медленно. Сначала появляется лишь некоторая тугоподвижность в конечностях, уменьшается гибкость суставов, возникают боль или общие затруднения при активных движения
Кроме болезни Паркинсона (первичного, или идиопатического паркинсонизма), которую связывают с  нейродегенеративным процессом, выделяют вторичный, или симптоматический паркинсонизм. Последний проявляется характерными двигательными расстройствами — понижением двигательной активности, замедлением произвольных движений и повышением мышечного тонуса — и обусловлен травматическими, токсическими или лекарственными повреждениями мозга, вирусным энцефалитом или цереброваскулярной патологией.
нейродегенеративным процессом, выделяют вторичный, или симптоматический паркинсонизм. Последний проявляется характерными двигательными расстройствами — понижением двигательной активности, замедлением произвольных движений и повышением мышечного тонуса — и обусловлен травматическими, токсическими или лекарственными повреждениями мозга, вирусным энцефалитом или цереброваскулярной патологией.
Специфичным как для болезни Паркинсона, так и вторичного паркинсонизма является снижение количества нейронов черной субстанции (одного из подкорковых ядер мозга), вырабатывающих и накапливающих дофамин — важнейший тормозной медиатор ЦНС. Нарушение синтеза дофамина приводит к дисбалансу тормозных и возбуждающих (ацетилхолиновых) нейромедиаторов, что, в свою очередь, обусловливает расстройство интегративных взаимоотношений между различными структурами головного мозга. Клинически это проявляется симптомами болезни Паркинсона. Следует отметить, что ЦНС хорошо адаптируется к небольшому дефициту дофамина, и клинические признаки паркинсонизма появляются только при более чем 70% снижении концентрации данного нейромедиатора относительно исходного уровня.
Проявления болезни Паркинсона
«Вы увидите тех, кто двигает дрожащими частями тела так, словно их головы или руки им не подвластны; и никакими усилиями они не могут унять эту дрожь», — так гениальный Леонардо да Винчи (1452–1519) писал в своих дневниках о людях, страдающих тремором. Вопреки распространенному мнению, а также убеждению самого Паркинсона, дрожание — характерный, однако не обязательный симптом заболевания. Тремор возникает вследствие ритмического сокращения мышц-антагонистов с частотой пять колебаний в минуту и более всего заметен в кистях рук. При выполнении пациентом направленного движения он становится менее выраженным или исчезает. Наряду с тремором к характерным проявлениям болезни Паркинсона относят гипокинезию, ригидность и постуральную неустойчивость (неустойчивое равновесие).
Гипокинезия (брадикинезия) — вынужденное замедление и снижение числа движений — внешне выражается прежде всего в значительном обеднении мимики и жестикуляции. Больные описывают гипокинезию как ощущение слабости и быстрой утомляемости. Особенно трудно им дается начало движения и его координация. На более поздних стадиях заболевания они отмечают затруднения при смене положения тела вo время сна; при пробуждении таким больным трудно встать с постели без посторонней помощи.
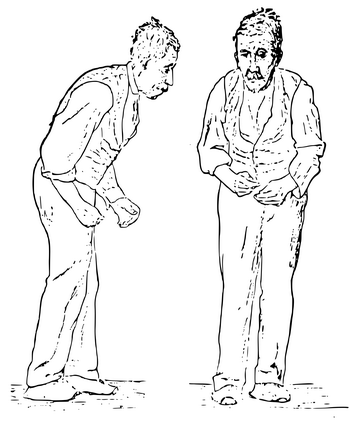 Ригидность клинически проявляется повышением мышечного тонуса. При исследовании пассивных движений у пациента ощущается ступенеобразное снижение тонуса в мышцах-антагонистах («феномен зубчатого колеса»). Повышенный тонус скелетных мышц может вызывать боль. Кроме того, он обусловливает характерную сутулую «позу просителя» у пациентов с болезнью Паркинсона.
Ригидность клинически проявляется повышением мышечного тонуса. При исследовании пассивных движений у пациента ощущается ступенеобразное снижение тонуса в мышцах-антагонистах («феномен зубчатого колеса»). Повышенный тонус скелетных мышц может вызывать боль. Кроме того, он обусловливает характерную сутулую «позу просителя» у пациентов с болезнью Паркинсона.
Постуральные рефлексы при болезни Паркинсона либо ослаблены, либо вовсе отсутствуют, в результате чего коррекция позы становится недостаточной, больные часто падают и вынуждены пользоваться опорными приспособлениями.
Диагноз болезни Паркинсона устанавливают при наличии как минимум двух из четырех описанных выше основных проявлений. В то же время следует учитывать и другие возможные признаки заболевания. Так, пациенты с болезнью Паркинсона ходят мелкими шаркающими шагами, однако иногда вынуждены для поддержания вертикальной позы ускорять шаг и даже переходить на бег, как бы «догоняя» свой центр тяжести. Исчезают содружественные качательные движения рук при ходьбе (ахейрокинез). В начале движения или перед преодолением препятствия больной может испытывать замешательство (так называемые эпизоды застывания). Оскудевает мимика, урежается мигание; речь становится монотонной из-за утраты координации в мышцах, участвующих в артикуляции. Нарушение координации в запястье и кисти обусловливает мелкий нечеткий почерк.
Снижение силы сокращения мочевого пузыря приводит к частым позывам к мочеиспусканию, а вялость кишечника — к запорам. Возможно также развитие ортостатической гипотензии (нарушение способности организма поддерживать в вертикальном положении обычный уровень артериального давления), себореи, слюнотечения, болевого синдрома.
Примерно у половины больных отмечаются проявления депрессии. По мнению ряда специалистов, она носит реактивный характер. Другие же рассматривают депрессию как симптом заболевания, в основе которого лежит разрушение дофаминергических нейронов в лимбической системе, играющей важную роль в формировании эмоций.
В 30% случаев на поздних стадиях заболевания наблюдаются снижение памяти, уменьшение интеллектуальной продуктивности, обучаемости и, в конечном счете, деменция. У 20% больных развиваются психотические нарушения — органический психоз с галлюцинаторно-параноидными проявлениями или хронический делирий (дезориентация во времени и месте, спутанность сознания, галлюцинации, бред).
Широкое применение нейролептиков в психиатрической и неврологической практике в различных странах мира привело к значительному росту частоты лекарственного (индуцированного лекарствами) паркинсонизма.
На поздних стадиях заболевания качество жизни пациентов с болезнью Паркинсона оказывается существенно сниженным. При грубых нарушениях глотания больные быстро теряют в весе. В случае длительной обездвиженности присоединяющиеся дыхательные расстройства и пролежни могут привести к летальному исходу.
Обычно выделяют пять стадий развития и, соответственно, степеней тяжести болезни Паркинсона:
1) односторонние симптомы паркинсонизма;
2) двусторонние симптомы паркинсонизма без нарушений равновесия;
3) присоединение умеренных нарушений равновесия;
4) значительное ограничение двигательной активности при сохранении возможности самостоятельно передвигаться;
5) больной прикован к постели или инвалидному креслу.
Лечение болезни Паркинсона
Терапия паркинсонизма: комплексно, последовательно, пожизненно
Современной медицине не известны методы излечения нейродегенеративных заболеваний, в том числе болезни Паркинсона. Поэтому терапия должна быть направлена на замедление прогрессирования заболевания, устранение патологических симптомов, улучшение качества жизни и предупреждение инвалидизации пациента.
Лекарственная терапия при болезни Паркинсона предполагает устранение биохимического дисбаланса (симптоматическая терапия), приостановление и уменьшение нейродегенеративного процесса (нейропротекторная терапия). С целью устранения дефицита дофамина назначают заместительную терапию или используют имеющиеся ресурсы дофаминергической системы.
 Заместительную терапию проводят препаратами леводопы — левовращающего изомера диоксифенилаланина (L-ДОФА), который является предшественником дофамина. По силе влияния на симптомы заболевания леводопасодержащие препараты превосходят все остальные противопаркинсонические средства. Современные леводопасодержащие препараты содержат вещества, блокирующие ассимиляцию леводопы на периферии, благодаря чему снижается риск развития таких побочных эффектов, как тошнота, рвота, тахикардия и кардиалгия. В то же время при их длительном приеме очень часто развиваются центральные побочные эффекты (нарушения моторики, у пожилых пациентов — психотические расстройства).
Заместительную терапию проводят препаратами леводопы — левовращающего изомера диоксифенилаланина (L-ДОФА), который является предшественником дофамина. По силе влияния на симптомы заболевания леводопасодержащие препараты превосходят все остальные противопаркинсонические средства. Современные леводопасодержащие препараты содержат вещества, блокирующие ассимиляцию леводопы на периферии, благодаря чему снижается риск развития таких побочных эффектов, как тошнота, рвота, тахикардия и кардиалгия. В то же время при их длительном приеме очень часто развиваются центральные побочные эффекты (нарушения моторики, у пожилых пациентов — психотические расстройства).
В целях стимуляции выброса дофамина в синаптическую щель и угнетения его обратного захвата используют амантадин. По некоторым данным, это лекарственное средство обладает также центральным холинолитическим и нейропротекторным эффектом. Селективную защиту эндогенного дофамина в нейронах обеспечивают препараты — ингибиторы ферментов, участвующих в разрушении дофамина: селегилин, толкапон, энтакапон. Возможно включение в схемы лечения болезни Паркинсона холинолитических средств (циклодола, норакина, беллазона). Они незаменимы в случае непереносимости препаратов дофаминергического ряда, однако часто вызывают серьезные побочные эффекты (снижение когнитивных функций, галлюцинации, деменцию).
К средствам, предположительно обладающим нейропротекторным действием при болезни Паркинсона, относят препараты с антиоксидантным эффектом, агонисты дофаминовых рецепторов, ингибиторы транспорта дофамина.
Снижение эффективности фармакотерапии и развитие тяжелых побочных эффектов при приеме противопаркинсонических препаратов являются показанием к применению нейрохирургических методов лечения. Целью стереотаксических деструктивных и стимуляционных операций является прерывание патологически функционирующих связей между различными структурами головного мозга.
Высокая степень инвалидизации при прогрессировании болезни Паркинсона, а также возникающие в связи с этим значительные социально-экономические проблемы обусловливают необходимость создания системы медико-социальной реабилитации. Она должна включать диспансерное наблюдение каждого больного группой специалистов (невролог, методист лечебной физкультуры, психотерапевт, социальный работник), специальные школы для пациентов и их родственников, психотерапевтические занятия и др.
В 1972 году на базе Института геронтологии НАМН Украины было открыто специализированное отделение по экстрапирамидным заболеваниям с Центром паркинсонизма. Оно стало первым подобным учреждением в бывшем СССР. С 1994 года активно работает Украинская ассоциация по борьбе с паркинсонизмом, защищающая интересы пациентов, страдающих этим тяжелым заболеванием.
Современной медицине пока не под силу полностью остановить прогрессирование болезни Паркинсона, однако своевременное лечение, как правило, позволяет на многие годы сохранить профессиональную и бытовую активность больного.












